成果介绍
运用基因指定区域泛编辑技术进行纳米抗体体外建库
转自:BDR生物设计研究 时间:2022-08-19
国家自然科学基金项目(批准号:82003261、81903187与82003261)、河南省自然科学基金项目((批准号:222300420513)和国家重点研发计划(批准号:2019YFA0906000)等资助下,本研究团队在运用基因编辑技术进行抗体体外建库研究领域取得进展。研究成果以“基因指定区域泛编辑技术进行纳米抗体体外建库(In vitro nanobody library construction by using gene designated-region pan-editing technology)”为题,于2022年08月19日发表于《生物设计研究》(BioDesign Research)。论文链接:DOI: 10.34133/2022/9823578。

【研究背景】
2019年研究团队成员一起讨论了运用合成生物学的方法在体外制备纳米抗体的可行性。要想实现纳米抗体的体外制备,首先需要解决纳米抗体体外建库的难题。进行有效的纳米抗体体外建库需要满足两个基本条件:第一,需要在纳米抗体的指定区域产生突变,即突变被限制在纳米抗体的3个高变区(又称互补决定区,CDRs),而稳定区保持不变。第二,突变不能是插入/缺失突变,这两种突变容易造成移码突变,从而导致纳米抗体功能丧失。
【研究内容】
哈佛大学刘如谦团队等开发的一系列碱基编辑器似乎能够满足这两点要求,如图1A所示,由传统gRNA引导的碱基编辑器(nCAS9+脱氨酶)能够定位于基因的指定区域,并在约30 bp的范围内通过碱基编辑增加相应区域的序列多样性。我们表达3个独立的分别导向纳米抗体3个CDRs区的gRNAs(图1B)去引导碱基编辑器,就会产生类似纳米抗体建库的效果。我们比较了由3种胞苷脱氨酶构建的碱基编辑器(CBE)的建库效果,发现两个AID突变体的碱基编辑效果较好(图1C-F)。
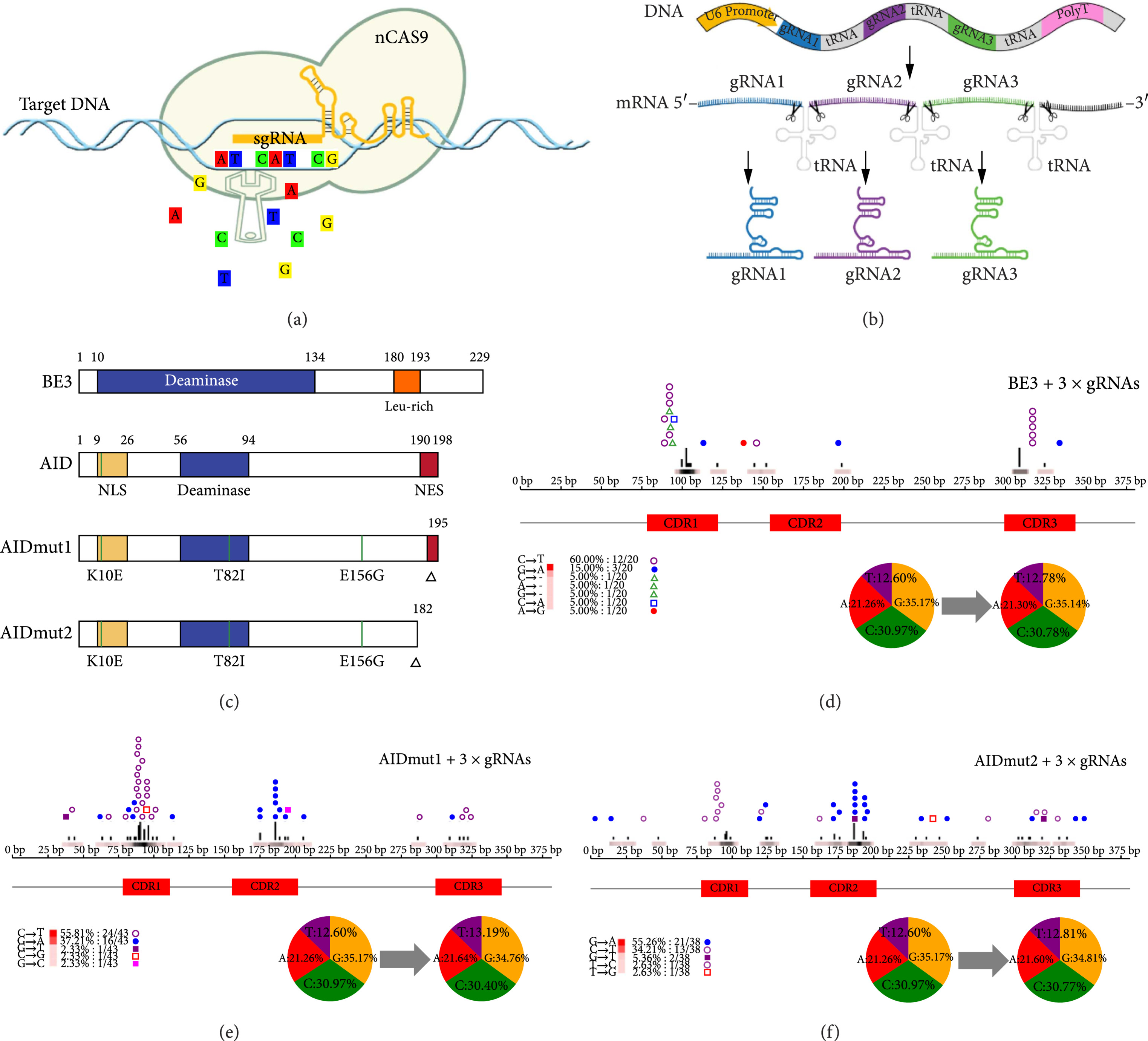
图1. 传统gRNA引导的碱基编辑器在基因指定区域的突变效果。
以上方案中,表达3个传统 gRNA 能够有效引导碱基编辑器到3个相应CDRs 区,并造成 gRNA 识别区及5′端毗邻区域的突变。但是,gRNA与靶标识别主要依靠5′端的 20 bp “种子序列(Seed Region)”,然而这 20 bp 种子序列中仅有 2 bp 的突变就会造成 约96%的 gRNA 引导功能丧失。碱基编辑器在每轮编辑过程中积累的突变数量是很少的,而很少的突变同时又造成了gRNA 引导功能丧失,所以传统gRNA 引导的碱基编辑器很难进行有效的纳米抗体建库。团队成员在讨论过程中也预想到了这一设计的缺陷,本文的第一作者通过详细了解CRISPR/Cas9基因编辑系统中gRNA的发现及改造历程,提出了拆分gRNA的设计构想,回归到原核生物中tracrRNA与crRNA的独立运行状态。同时,运用tracrRNA与crRNA间杂交序列的可编程性,设计出一种可持续引导碱基编辑器到基因指定区域的自组装gRNA(self-assembling gRNA)。在本次改进型方案中不再直接表达3个完整的gRNA序列,而是只表达gRNA的tracrRNA部分(即截短型gRNA,简称gRNAΔ),并且将gRNAΔ的5′端与crRNA相互补的序列(约14 bp)修改为能够与纳米抗体mRNA三个CDR区3′端的稳定区相互识别的序列(如图2A,2B所示)。当gRNAΔ与纳米抗体的mRNA结合之后,真核细胞中也有相应的RNA酶对gRNAΔ:mRNA进行切割加工,最终得到完整的自组装gRNA(图2B)。由于这种设计能够使gRNA的种子序列(Seed region)始终来自于纳米抗体的三个CDR区,并且三个CDR区突变之后gRNA种子序列也能够相应的发生变化,从而使这种自组装gRNA始终靶向自身的种子序列来源区,并在纳米抗体三个CDR区产生持续突变,从而实现纳米抗体的持续突变建库。
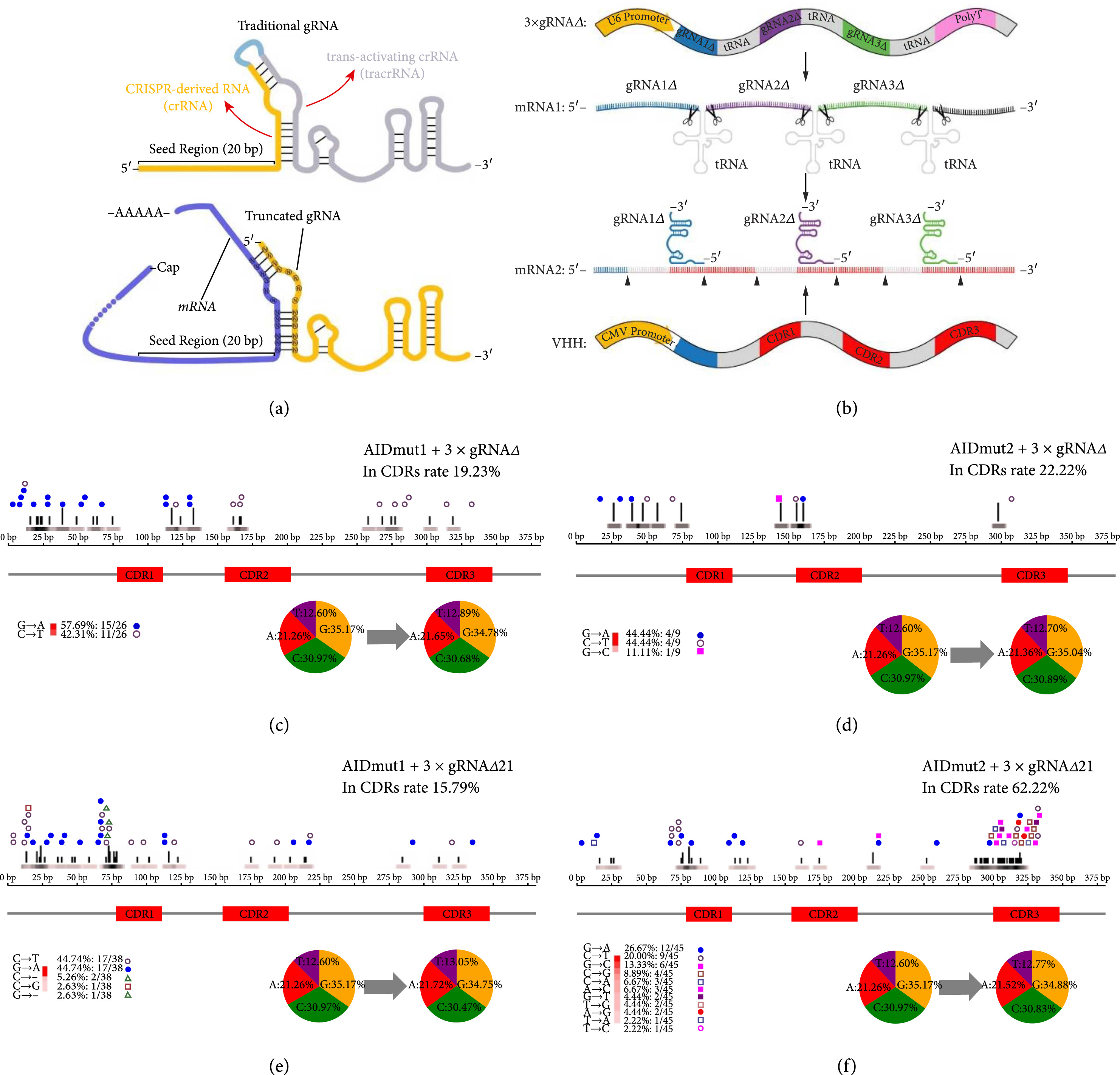
图2. 传统gRNA与自组装gRNA对种子序列区突变耐受性对比。
虽然我们设计了自组装gRNA,并初步展示出了抗突变干扰并进行迭代突变建库的潜力。但是,要最终实现纳米抗体体外建库,除了高效的CBE碱基编辑器,我们还需要高效的ABE碱基编辑器。同时还需要解决对突变区域范围的精准控制、解决脱靶造成的细胞毒性以及开发基于真核细胞的纳米抗体展示及筛选技术等难题。
【研究意义】
这种基于迭代突变/进化技术的深入开发,在未来对智能化细胞的设计也将产生重要影响,这将使得细胞在接收我们输入的指令后不再单纯的输出我们已知的或预设的信号,而是有能力输出经过细胞“思考”、“判断”及“优化”后的信号。
新乡医学院生命科学技术学院副教授牛志远为该文章第一作者,朱武凌教授为通讯作者。测序结果分析采用了郭长江博士编写的Python脚本。
(文/牛志远 图/牛志远)
